Die Thermodynamik befasst sich mit allem, was mit dem Austausch von Energie zu tun hat, nicht nur mit Wärme (was das Präfix thermo vermuten lassen würde).
Sie wird durch Prinzipien geregelt, die unbedingt eingehalten werden müssen, es sind Gesetze, die von der Natur auferlegt werden.
Diese Prinzipien sind absolut, sie sind keine widerlegbaren wissenschaftlichen Theorien (man müsste in einem anderen Universum leben, um zu wissen, dass sie möglicherweise anders sind).
Wenn sich zwei Systeme im thermodynamischen Gleichgewicht mit einem dritten befinden, dann befinden sie sich auch untereinander im Gleichgewicht.
Wie Maxwell es ausdrückte. "Alle Wärme ist von derselben Art".
Die Energie bleibt erhalten.
Die innere Energie eines Systems ändert sich, wenn Wärme in das System hinein oder aus ihm heraus fliesst.
Mit anderen Worten: Arbeit zu produzieren, ohne Energie zuzuführen, ist unmöglich.
Die Entropie eines isolierten Systems nimmt nie ab.
Im Gleichgewicht befindet sich ein solches System mit seiner maximalen Entropie.
Mit anderen Worten:
Die Unordnung in einem System kann nur zunehmen.
Oder:
Die verfügbare Energie (zur Umwandlung, z.B. um mechanische Arbeit zu verrichten) eines isolierten Systems ist geringer als seine innere Energie.
Oder:
Die maximale Effizienz eines Verbrennungsmotors ist η = 1-TF/TC ,
wobei TF die absolute Temperatur [in Kelvin] des kalten Reservoirs (Senke) und TC die des heissen Reservoirs (Quelle) ist.
In vulgäreren Worten:
Ein Haufen Steine, der in die Luft geworfen wird, hat eine sehr, sehr geringe Chance, in Form einer Kathedrale wieder aufzufallen.
Die Entropie einer reinen Substanz ist Null bei der Null Temperatur (T= 0 Kelvin).
In vulgäreren Worten:
Die maximale Ordnung ist erreicht, wenn nichts geschieht oder existiert.
Nullter (dritter) Hauptsatz der Thermodynamik *
Zwei Systeme im thermischen Gleichgewicht mit einem dritten, stehen auch unter sich im thermischen Gleichgewicht.
Systeme im thermischen Gleichgewicht haben dieselbe Temperatur.
Systeme die nicht im thermischen Gleichgewicht stehen, haben unterschiedliche Temperaturen.
Praktische Bedeutung: Wärme kann nur von einem Medium höherer zu einem Medium tieferer Temperatur fliessen.
Anmerkung (*): Historisch gesehen hat man zuerst den 1. Hauptsatz (Energie-Erhaltung) und den 2. Hauptsatz (Irreversibiltät der natürlichen Prozesse) formuliert und nahm die oben ausgedrückte Erfahrungstatsache als selbstverständlich hin. Erst später ist man zur Erkenntnis gelangt, dass es sich hier tatsächlich um eine fundamentale und grundsätzliche Erkenntnis der Thermodynamik handelt, die den beiden bereits formulierten Sätzen vorangeht. Daher rührt die eigenartige Bezeichnung „nullter“ Hauptsatz. Jedoch, oft wird dies auch als der 3. Hauptsatz der Thermodynamik bezeichnet.
Beispiel dazu: Man denke sich eine Badewanne mit zwei Wasser- Einläufen, an jedem Ende der Wanne einen. Der eine mit Heisswasser (rot eingefärbt) der andere mit Kaltwasser (blau eingefärbt). Die eingefüllten Wassermengen (kalt und heiss) werden in ein thermisches Gleichgewicht übergehen und dieselbe Temperatur (Farbe) – die Mischtemperatur (Mischfarbe) – erreichen.
Es gibt dazu verschiedene Formulierungen, sehr mathematisch-abstrakte und auch mehr allgemein verständliche:
Durch den Einbezug von mechanischer Energie, Wärme, chemischer und elektrischer Energie erhält der Satz eine umfassende Bedeutung: Der Unmöglichkeit eines Perpetuum Mobile der 1. Art.
Zweiter Hauptsatz der Thermodynamik
Ist möglicherweise der komplexeste der drei grundsätzlichen thermodynamischen Gesetze. Auch dazu gibt es verschiedene Formulierungen, sehr mathematisch-abstrakte und auch mehr allgemein verständliche:
Zur Weiterführung des Beispiels unter „Nullter Hauptsatz“: Wir beobachten dabei noch folgendes: Die Wärme fliesst vom Medium höherer Temperatur (Heisswasser, rot) zum Medium niedriger Temperatur (Kaltwasser, blau) und heizt dieses auf die Mischtemperatur. Wir wissen aus Beobachtung, dass die Umkehrung nicht möglich ist, weder würden sich die Wassermengen wieder von sich aus in eine rot- und blau- Zone entmischen, noch würden sich die Temperaturen in heiss und kalt separieren. Wäre dies möglich, hätten wir ein Perpetuum Mobile der 2. Art. Das Beispiel zeigt die Irreversibilität natürlicher Prozesse.
Anmerkung: Die Entropie (s [kJ/(kg*K)] ist die durch den 2. Hauptsatz definierte Zustandgrösse eines Stoffes (Gas, Flüssigkeit).

Der maximale (erreichbare) thermische Wirkungsgrad (ɳ) errechnet sich:
ɳc = 1 – (TII/ TI)
TI = Temperatur bei welcher einem thermischen Prozess Wärme zugeführt wird (in [K]).
TII = Temperatur bei welcher einem thermischen Prozess Wärme abgeführt wird (in [K])

Beispiel aus Geothermie: TI = 135 [C] -> 408 [K] TII = 20 [C] -> 293 [K]
ɳc = 1 – (293/408)
ɳc = 28 (%)
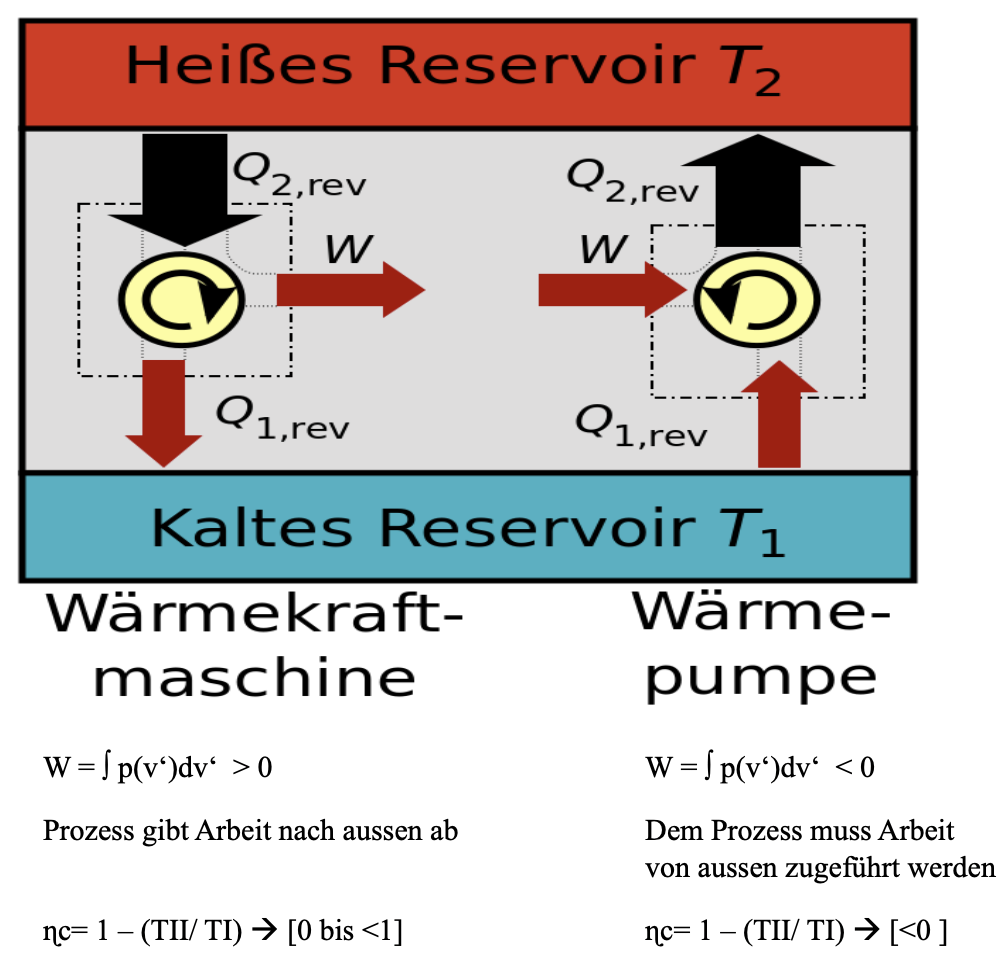
Der Carnot Prozess als Wärmekraftmaschine oder deren Umkehrung: die Wärmepumpe („der Kühlschrankprozess“).
Carnot Wirkungsgrad als Asymptote für reale Energieprozesse:
Der (damals) gedankliche (geniale!) Ansatz von Carnot beruht jedoch auf der Annahme von Reversibilität: Eine isentrope Verdichtung oder –Expansion gibt es nicht, es sind beispielsweise immer systeminterne Reibungen vorhanden (= irreversible Verluste:
Wenn man eine Masse (m) auf einer ebenen Fläche von A nach B verschiebt gibt es Reibungsverluste entsprechend dem Ansatz:
Rv = Masse * Gravitationskonstante * Reibungskoeffizient * Strecke (A->B).
Wenn ich dieselbe Masse von B nach A zurückschiebe, dann verliere ich wiederum Rv, Rv ist immer > 0!
So liegt der im realen thermischen Prozess bestenfalls erreichbare Wirkungsgrad immer unterhalb vom Carnot-Wirkungsgrad :
ɳc > ɳth real
Die Differenz zwischen ɳc und ɳth real ist auch desto grösser, je geringer die Differenz zwischen TI und TII ist. Dies aus folgendem Grund:
Anmerkung: Ich erinnere dabei an den Artikel „das ganze Meer als Sonnenkollektor“ den die NZZ im Frühjahr 2014 unter „Forschung“ publizierte. Da wurde ein Prozess auf Schwimmplattformen in den Tropen beschrieben, wo zwischen rund 33 [deg C] an der Meeresoberfläche und 4 [deg C] in tiefen Schichten (mehr als 400m) gearbeitet werden soll. Das gäbe einen
ɳc = 0.095 !
Ein kapitaler Unsinn, wo ohne weiteres nachrechen „Energy return on Energy invested“ nie aufgehen würde.
Noch sei daran erinnert, die Physik baut auf 5 axiomatischen Dimensionen auf (MKSA System):

Alle anderen weiteren physikalischen Dimensionen sind davon abgeleitet.
Über Dimensionsanalysen lassen sich energetische Überlegungen verknüpfen und vergleichen: Carnot, resp die Thermodynamik gilt universell!
Emanuel Höhener, 24. April 2021
Diese physikalische Grösse ist sehr unbekannt. Sie ist intensiv, man kann sie nicht in Massen akkumulieren, obwohl man sagt, dass sie schwerlastig oder leicht sein kann. Sie braucht Materie, sonst gäbe es keine Temperatur, da sie den Zustand der Unruhe darstellt, in dem sich diese Materie befindet,
Dies wäre der absolute Nullpunkt, an dem nichts existiert.

Nachstehend
wird diese Technologie zur Erzeugung von elektrischem Strom durch die
Kombination von Gas und Dampf vorgestellt, die den Carnot-Zyklus angreift, um
ein Optimum zu erzielen.
Dieser Text unseres Präsidenten Emanuel Höhener ist
zeitlos und immer noch hochaktuell.